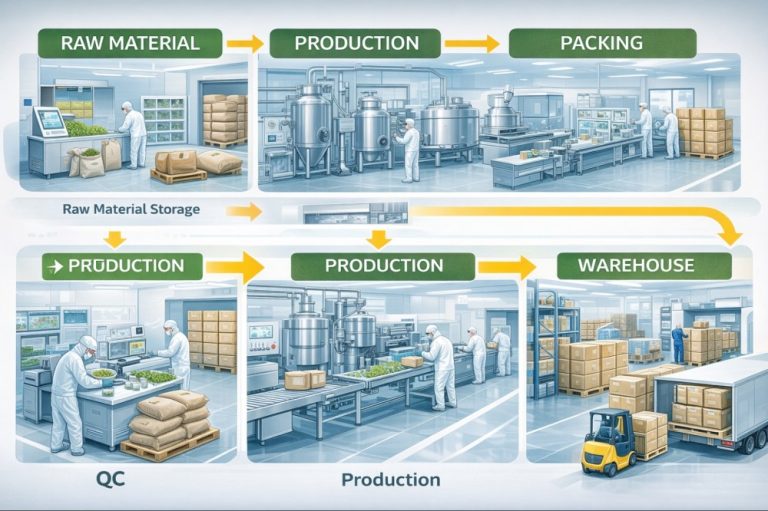
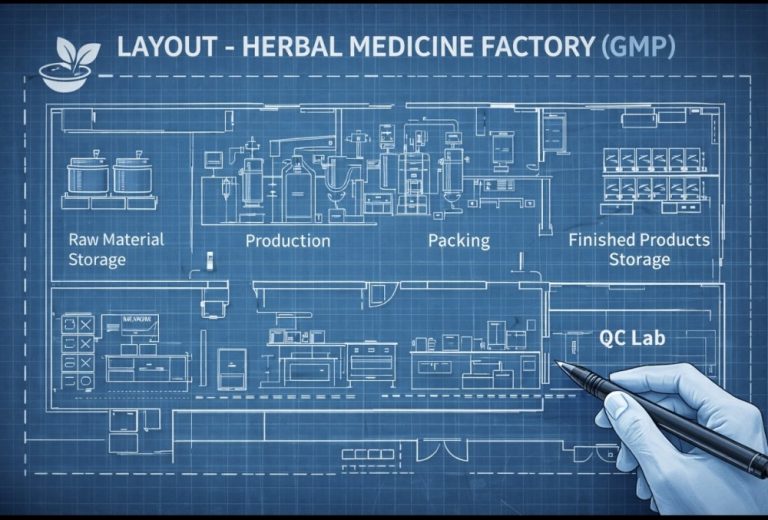
การได้รับรองมาตรฐาน GMP (Good Manufacturing Practice) และ PIC/S ถือเป็นความสำเร็จครั้งสำคัญของโรงงานผลิตยาและอาหารเสริม เป็นเครื่องยืนยันถึงความมุ่งมั่นในคุณภาพและความปลอดภัย อย่างไรก็ตาม บ่อยครั้งที่โรงงานที่ได้รับการรับรองแล้วกลับพบว่ายังคงมี ปัญหาในการปฏิบัติงาน จริง ไม่ว่าจะเป็นเรื่องความไม่สอดคล้องกับข้อกำหนด, การควบคุมคุณภาพที่ยังไม่สม่ำเสมอ, หรือการที่บุคลากรยังไม่เข้าใจถ่องแท้ถึงหลักการที่ถูกต้อง
QMSFactory.com เข้าใจถึงช่องว่างเหล่านี้ และพร้อมชี้ให้เห็นถึงปัญหาที่พบบ่อย พร้อมแนวทางแก้ไข เพื่อให้การลงทุนในการขอรับรองของคุณเกิดประโยชน์สูงสุด
ปัญหาที่พบบ่อยหลังการรับรอง GMP PIC/S
* ความเข้าใจไม่ถ่องแท้ของบุคลากร:
* ปัญหา: แม้จะมีการอบรมในช่วงแรก แต่พนักงานบางส่วนอาจยังไม่เข้าใจหลักการและเหตุผลเบื้องหลังของข้อกำหนด GMP/PIC/S อย่างลึกซึ้ง ทำให้การปฏิบัติตามเป็นเพียงการทำตามขั้นตอน ไม่ใช่ความเข้าใจที่แท้จริง
* ผลกระทบ: นำไปสู่การละเลยขั้นตอนสำคัญ, การบันทึกข้อมูลที่ไม่ครบถ้วน, หรือการตัดสินใจที่ผิดพลาดเมื่อเกิดสถานการณ์ที่ไม่คาดคิด
* ขาดการทบทวนและปรับปรุงระบบอย่างต่อเนื่อง:
* ปัญหา: หลายโรงงานมองว่าการได้ใบรับรองคือปลายทาง ทำให้ละเลยการทบทวนประสิทธิภาพของระบบ QMS และ GMP/PIC/S อย่างสม่ำเสมอ หรือไม่ได้ปรับปรุงให้เข้ากับสถานการณ์และเทคโนโลยีที่เปลี่ยนแปลงไป
* ผลกระทบ: ระบบที่เคยดีอาจล้าสมัยหรือไม่เหมาะสมกับสภาพปัจจุบัน ทำให้เกิดปัญหาซ้ำซาก หรือพลาดโอกาสในการพัฒนา
* การควบคุมการเปลี่ยนแปลง (Change Control) ที่อ่อนแอ:
* ปัญหา: เมื่อมีการเปลี่ยนแปลงใดๆ ไม่ว่าจะเป็นวัตถุดิบ, กระบวนการ, เครื่องจักร, หรือแม้กระทั่งบุคลากร หากไม่มีการบริหารจัดการการเปลี่ยนแปลงที่ดีพอ อาจส่งผลกระทบต่อคุณภาพผลิตภัณฑ์โดยไม่รู้ตัว
* ผลกระทบ: ความเสี่ยงที่ผลิตภัณฑ์จะไม่ได้มาตรฐานเพิ่มขึ้น, ต้องแก้ไขงาน (Rework), หรืออาจถึงขั้นถูกเรียกคืน (Recall)
* การบริหารจัดการเอกสารและบันทึกไม่เป็นระบบ:
* ปัญหา: แม้จะมีการจัดทำเอกสารตามข้อกำหนด แต่การจัดเก็บ, การค้นหา, การควบคุมเวอร์ชัน, หรือการบันทึกข้อมูลไม่เป็นไปตามมาตรฐาน ทำให้การตรวจสอบย้อนกลับทำได้ยาก หรือเกิดความผิดพลาดในการใช้งาน
* ผลกระทบ: เสียเวลาในการค้นหาข้อมูล, เกิดข้อผิดพลาดจากเอกสารล้าสมัย, หรือไม่สามารถพิสูจน์ได้เมื่อเกิดปัญหา
* วัฒนธรรมองค์กรที่ไม่เอื้อต่อการปฏิบัติตามมาตรฐาน:
* ปัญหา: หากผู้บริหารไม่แสดงออกถึงความสำคัญของ GMP/PIC/S อย่างชัดเจน หรือไม่มีการสร้างแรงจูงใจให้พนักงานปฏิบัติตาม จะทำให้เกิดความรู้สึกว่า “ทำๆ ไปให้มันจบๆ”
* ผลกระทบ: การไม่ปฏิบัติตามมาตรฐานกลายเป็นเรื่องปกติ, คุณภาพลดลง, และอาจนำไปสู่การไม่ผ่านการตรวจประเมินในรอบต่อไป
แนวทางแก้ไขและพัฒนาเพื่อการปฏิบัติที่ยั่งยืน
* การอบรมเชิงลึกและต่อเนื่อง: จัดอบรมที่ไม่ใช่แค่การบอกว่า “ทำอะไร” แต่เน้นที่ “ทำไมต้องทำ” และ “ทำอย่างไรให้ดีขึ้น” รวมถึงการอบรมหน้างาน (On-the-job training) และการจัดทำคู่มือที่เข้าใจง่าย
* สร้างทีม Internal Audit ที่เข้มแข็ง: ฝึกอบรมบุคลากรภายในให้เป็นผู้ตรวจสอบ (Auditor) ที่ดี เพื่อประเมินระบบอย่างสม่ำเสมอและค้นหาจุดที่ต้องปรับปรุงก่อนที่หน่วยงานภายนอกจะเข้ามาตรวจ
* ใช้เทคโนโลยีช่วยเสริม: พิจารณาการนำระบบ Digital QMS, e-Logbook, หรือระบบบริหารจัดการเอกสารอิเล็กทรอนิกส์ (EDMS) มาใช้ เพื่อลดข้อผิดพลาดจากการบันทึกด้วยมือ และเพิ่มประสิทธิภาพในการเข้าถึงข้อมูล
* ส่งเสริมวัฒนธรรมคุณภาพจากผู้นำ: ผู้บริหารต้องเป็นต้นแบบและแสดงให้เห็นถึงความมุ่งมั่นในคุณภาพอย่างสม่ำเสมอ พร้อมทั้งให้การสนับสนุนทรัพยากรที่จำเป็น และให้รางวัลแก่พนักงานที่ปฏิบัติดี
* ปรึกษาผู้เชี่ยวชาญภายนอก: หากยังพบปัญหาที่ไม่สามารถแก้ไขได้เอง การปรึกษา ที่ปรึกษา GMP PIC/S ที่มีประสบการณ์ จะช่วยวิเคราะห์และให้คำแนะนำที่ตรงจุด พร้อมแนวทางแก้ไขที่ได้รับการพิสูจน์แล้ว
การได้รับการรับรอง GMP PIC/S เป็นเพียงจุดเริ่มต้น การคงไว้ซึ่งมาตรฐานและการปฏิบัติอย่างต่อเนื่องในทุกวันต่างหากที่เป็นความท้าทายที่แท้จริง QMSFactory.com พร้อมเป็นพันธมิตรของคุณในการช่วยวิเคราะห์ปัญหา วางแผนแก้ไข และยกระดับระบบการปฏิบัติงานของโรงงานคุณให้เป็นไปตามมาตรฐานสูงสุดได้อย่างยั่งยืน
หากโรงงานของคุณกำลังเผชิญกับปัญหาในการปฏิบัติตามมาตรฐาน GMP PIC/S หรือต้องการคำปรึกษาเพื่อการปรับปรุงอย่างต่อเนื่อง
ติดต่อ QMSFactory.com วันนี้!